
功能微纳米材料因其丰富的光、电、磁学特性和良好的生物相容性,在体外诊断、分子影像、疾病治疗等生物医学领域有广泛的应用。东纳生物在多年研发积累以及产业化应用的过程中,围绕微纳米材料技术成功建成三大创新研发平台及应用解决方案,将为广大客户提供优质的生物医学微纳米材料产品、科研定制服务以及医疗产品研发服务。
东纳生物拥有系列高性能生物医用创新产品,包括各种功能的铁基磁性纳米颗粒、金纳米颗粒、银纳米颗粒、量子点、纳米乳、纳米高分子载体、智能磁响应凝胶、磁性微气泡、磁性石墨烯、广泛应用于细胞磁标记示踪、基因磁转染、荧光标记、药物载体、生物传感、磁共振成像、CT造影、超声成像、光声成像、暗场成像、表面增强拉曼检测、光热治疗和磁感应热疗等领域,为广大生命科学与医学研究以及诊疗应用开发提供强有力的支撑。在此基础上,具备从材料制备、表面修饰、多模态多功能纳米体系构建,到细胞实验、动物实验,以及开发体外诊断试剂、分子影像探针、多功能诊疗制剂应用的全链条研发服务。
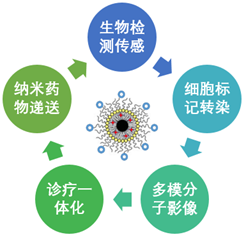
功能纳米材料及诊疗应用创新研发与服务平台
基于高性能磁珠表面的抗原-抗体、DNA互补、亲和素-生物素、酶-底物等特异性反应,可用于识别、捕获、标记、分离、检测、信号放大、催化等功能构建,包括核酸提取、文库构建、DNA探测与传感、纯化PCR产物、核酸转染、抗体纯化、细胞分选与检测、特定蛋白分离、糖蛋白分离、GST融合蛋白分离、酶联免疫检测、化学发光检测、免疫沉降-蛋白质免疫印记分析、多元免疫检测、病原微生物捕获与检测、酶固定化与级联酶固定等众多应用。围绕磁性微球,东纳生物专家团队可以根据客户需求提供个体化的综合解决方案及定制服务,满足客户在分离、检测等领域的创新应用。
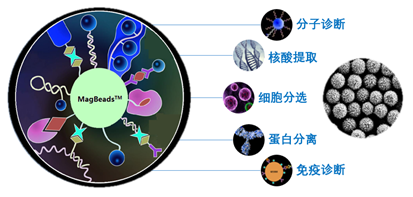
磁性微球及体外诊断应用创新研发与服务平台
3. 荧光微球及POCT快速诊断创新研发与服务方向
建立了基于高性能荧光微球、纳米酶及多重级联信号放大技术,并通过纳米颗粒表面非特异性修饰和取向抗体偶联技术,大大提高了检测灵敏度和特异性,为实现疾病标志物的快速即时检测提供了强有力的工具;同时开发了桌面型和便携式检测设备,具备测量快速准确、精确内部外部双重质控、无线传输数据和远程监控的特色和优势,可同时测量蛋白、核酸等多种指标,广泛适用于科研、动植物快速检测等领域。东纳生物多年的体外诊断试剂研发经验可以为客户提供各种诊断试剂与设备的研发服务、关键原料加工与改性服务、半成品生产服务以及检测服务。
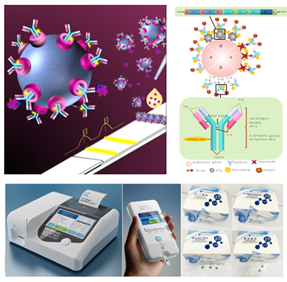
荧光微球及POCT快速诊断创新研发与服务平台
▌微纳米材料表面有机分子或高分子修饰:
在已有在售产品的基础上,根据客户需求将一些功能有机分子或高分子通过静电组装、化学共价偶联等方法偶联到纳米材料表面。
▌基于纳米材料的复合高分子制备:
如磁性海藻酸钠水凝胶或微球、磁性聚乳酸微球、电纺磁性纳米纤维等。
▌载药纳米材料的制备:
根据客户需求将油溶性或水溶性药物分子负载到纳米材料或脂质体中,如阿霉素、紫杉醇等。
▌生物靶向性小分子修饰的磁性纳米颗粒制备:
通过EDC/NHS偶联化学将生物靶向性小分子,如RGD、叶酸、半乳糖、葡萄糖等,偶联到纳米材料表面,构建靶向纳米探针。
▌抗体偶联纳米材料制备:
通过酰胺键、二硫键等生物相容性偶联方法将生物靶向性抗体等蛋白分子,如美罗华单抗(针对CD20)、西妥昔单抗(针对EGFR)、曲妥珠单抗(针对HER2)等,偶联到纳米材料表面,构建靶向纳米探针。
▌ 酶固定微纳米材料:
通过酰胺键、二硫键等生物相容性偶联方法将酶分子偶联到纳米材料表面,如辣根过氧化物酶、过氧化氢酶、蛋白水解酶等,可赋予稳定化、磁分离、增强酶活性等功能。
▌RNA/DNA负载纳米材料:
通过静电、疏水相互作用及装载等方法将RNA或DNA与纳米材料构建成组装体,对RNA或DNA进行转染或输运。
▌包含纳米材料的纳米乳液制备:
通过超声乳化方法将纳米材料或其他成分装载到纳米乳中,形成稳定的载体。
▌多模态、多功能纳米材料系统的构建:
根据客户需求将磁性、光学、超声成像单元及药物分子进行组装和复合,构建用于多模态成像与多功能诊疗的纳米结构。
▌基于高分子材料的纳米药物载体(如高分子胶束、聚合物纳米粒、凝胶等)构建
如:PGA-PLGA、壳聚糖、葡聚糖、透明质酸、海藻糖等等。
▌磁性微球表面修饰各种核酸探针、抗体等特定蛋白质
用于发展分子诊断、免疫诊断、细胞分选等检测方法与技术。
▌帮助体外诊断企业进行磁性微球在化学发光、分子诊断等各种诊断试剂开发中的验证和优化工作,确保客户更优化地应用我们的产品。
▌荧光成像用PEG话石墨烯量子点
石墨烯量子点在生物成像方面极具应用前景,在理论和实验上都已证实,量子限制效应和边效应可诱导石墨烯量子点发出荧光。在生物医学研究领域中,常用荧光标记来标定研究对象,却会因为过长的激发时间使得荧光失效被称为光漂白使得一般荧光剂在生物医学上的应用受到限制。石墨烯量子点拥有稳定的荧光光源,从而也被称为“永不淬灭的荧光”。通过PEG化修饰,能进一步提高石墨烯量子点水溶性、生物相容性和体内循环时间,同时可通过结合靶向分子来提高PEG化石墨烯量子点的主动靶向能力。
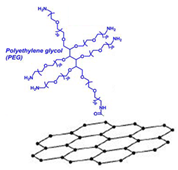
PEG化石墨烯量子点示意图
▌核医学分子成像探针载体——DOTA修饰的PEG化纳米材料
DOTA分子是一种十二元四氮杂大环配体的金属元素螯合剂。通过在PEG化纳米材料表面结合DOTA分子来螯合放射性核素,将核医学检测与磁共振,光学成像以及光声成像等结合起来。在实现多模态成像的同时可以掺入靶向分子及药物来达到诊疗一体化的效果。
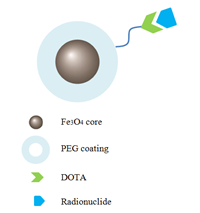
DOTA修饰的PEG化纳米颗粒示意图
▌肿瘤靶向荧光/MRI双模态纳米探针
将cy5.5荧光分子负载到磁性脂质纳米颗粒双层中来实现荧光/MRI双模态造影,再通过化学偶联剂交联cRGD来达到靶向肿瘤新生血管的目的。
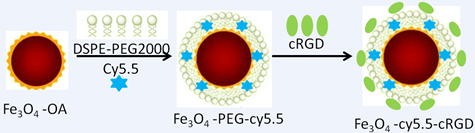
新生血管靶向的荧光/MRI双模态纳米探针
▌多功能脂质体构建
通过在脂质体内部负载药物多肽和荧光分子以及在外部偶联靶向分子来实现诊断和靶向治疗的目的。
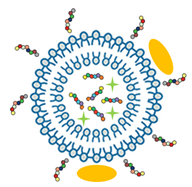
多功能脂质体构建结构图
▌超声/磁共振双模态纳米探针
携带磁性纳米颗粒的微气泡载体材料,由于兼具优良的磁学特性和声学特性,逐渐发展成为一个集超声/磁共振双模式显影、基因及药物的靶向传输与一体的多功能诊疗一体化平台。
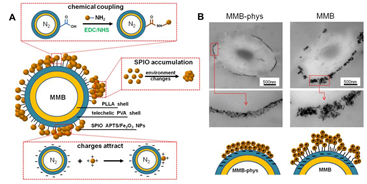
超声/磁共振双模态纳米探针模型及透射电镜图
▌基于磁性脂质纳米颗粒的肿瘤诊疗一体化
基于PEG化磁性纳米颗粒的肿瘤靶向成像纳米探针兼顾磁共振造影和磁感应热疗的功能,同时可负载脂溶性荧光分子进行荧光成像,以及联合纳米颗粒磁感应的热成像,实现多模态成像指导下的肿瘤靶向治疗。这些研究目前已在肿瘤诊疗领域显示出良好的优势和临床应用价值。
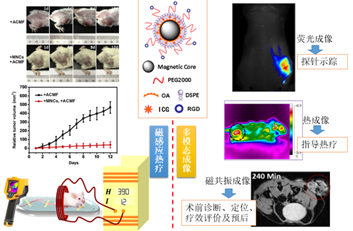
新生血管靶向的肿瘤多模态成像及磁感应热疗
东纳生物以磁性引领行业,以微小促您成功,以细微彰显服务,将为客户带来全新的使用体验和全面的定制服务方案。
“助力科研创新,帮助客户成功”